作者:李静宜、周胜敏
近年来研究发现,胞内pH(pHi)作为信号分子决定细胞生老病死,被视为第二信使,引起学术界广泛关注。为研究pHi影响细胞命运的分子机制,多款能实时检测pHi的基因编码型荧光探针应运而生。这些探针大都由普通荧光蛋白及其突变体改造而成,虽能感应pH变化,但灵敏度尚待提高。近期3044am永利集团纳米生物工程实验室周胜敏副教授课题组构建了一款超灵敏基因编码型pH探针,并基于该探针的检测优势,发现了一种全新生物学现象。相关成果以“Genetic engineering of circularly permuted yellow fluorescent protein reveals intracellular acidification in response to nitric oxide stimuli”为题发表于氧化自由基生物学领域高影响力期刊Redox Biology上。
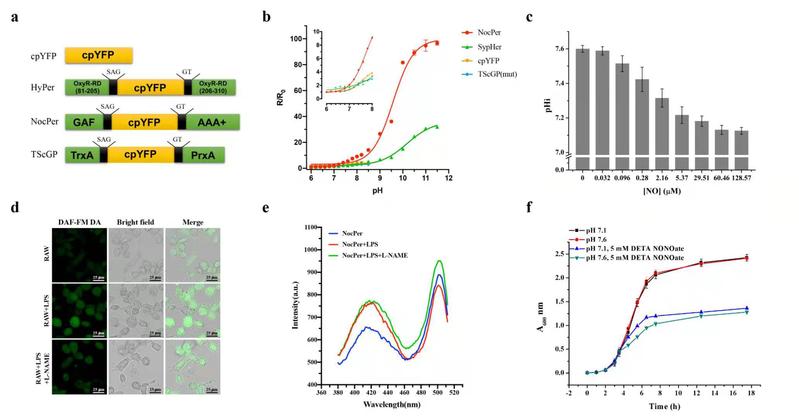
圆排列环状荧光蛋白(cpFP)相较于普通荧光蛋白(FP)展示出更高的pH敏感性,具备检测pH的先天优势,但由于存在荧光峰易迁移、稳定性欠佳,尤其是仅具有单峰,限制了其作为比例型探针的应用潜力。周胜敏课题组在黄色cpFP(cpYFP)分子的碳、氮端分别连接了一氧化氮(NO)感受蛋白NorR的失活突变体蛋白片段(图a),发现该探针虽不能在体外感应NO,但可响应pH的细微变化,且具有双峰,其灵敏度为常用pH探针pHluorin的3倍(图b),因此是一款比例型超灵敏pH探针,命名为NocPer。进一步研究发现,NocPer虽非NO探针,但在大肠杆菌体内却能响应胞外NO的刺激,暗示NO刺激可能激发pHi变化(图c)。最后通过多重实验验证了“NO刺激引起pHi下降”这一假说,并阐述其所涉的机制,NO通过抑制呼吸链复合物III的活性,限制了质子的膜外搬运,引起pHi下降。研究还证实在感染人体过程中,巨噬细胞释放NO(图d),此条件下微生物维持低pHi(图e),是病原菌的一种自我保护策略(图f)。
该研究设计的探针,既充分发挥了cpYFP在pH感应灵敏度上的天然优势,又改善了其原有信号上的短板,同时展示了超灵敏pH探针在生物学新现象发现中的重要性。
公司邓海涛(硕士)、李静宜(博士)为论文共同第一作者,3044am永利集团周胜敏副教授为论文通讯作者。该研究得到了王平教授的悉心指导,并受到国家自然科学基金、科技部重大专项、科技部国际合作专项等项目的资助。
原文链接:https://www.sciencedirect.com/science/article/pii/S2213231721000914